IF 42.5高分力作:泓迅生物技術(shù)助力破解CRISPR起源之謎?

近日,國際頂級(jí)期刊Cell(IF :42.5)發(fā)表了一篇題為《Functional RNA splitting drove the evolutionary emergence of type V CRISPR-Cas systems from transposons》的重磅研究。該研究由中國科學(xué)院遺傳與發(fā)育生物學(xué)研究所團(tuán)隊(duì)完成,首次系統(tǒng)揭示了一類名為“TranC”的轉(zhuǎn)座子-CRISPR中間系統(tǒng),并提出了“功能性RNA分裂”是驅(qū)動(dòng)V型CRISPR系統(tǒng)從轉(zhuǎn)座子中演化而來的關(guān)鍵機(jī)制。

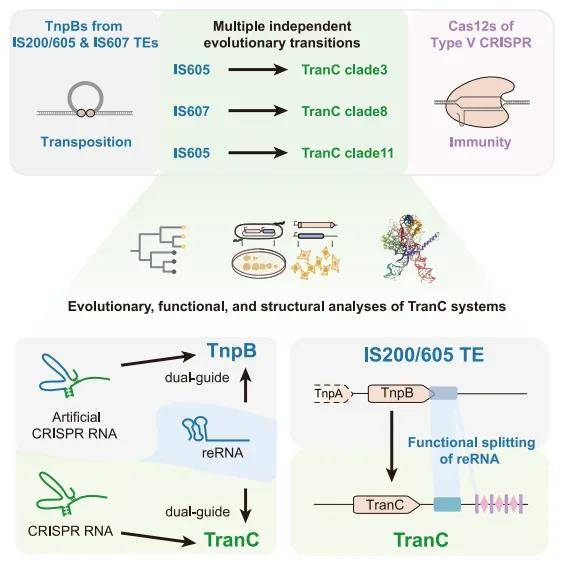
CRISPR系統(tǒng)從何而來?
CRISPR-Cas系統(tǒng)是細(xì)菌和古菌的“適應(yīng)性免疫系統(tǒng)”,其核心蛋白如Cas9和Cas12已被廣泛用于基因編輯。長期以來,科學(xué)家認(rèn)為這些系統(tǒng)起源于轉(zhuǎn)座子(跳躍基因)的“馴化”。尤其是Cas12,被認(rèn)為是從轉(zhuǎn)座子編碼的TnpB蛋白演化而來。然而,這一演化過程的具體機(jī)制一直是個(gè)未解之謎。
核心發(fā)現(xiàn)與創(chuàng)新
本研究的突破性在于,它精準(zhǔn)地捕捉并證實(shí)了這一進(jìn)化過程的中間狀態(tài),其核心發(fā)現(xiàn)可凝練為以下四點(diǎn):
1.發(fā)現(xiàn)真正的進(jìn)化中間體
“TranC”系統(tǒng):研究團(tuán)隊(duì)通過創(chuàng)新的多策略計(jì)算生物學(xué)挖掘,從海量基因組數(shù)據(jù)中鑒定出146個(gè)TranC(Transposon-CRISPR intermediate)蛋白。它們兼具祖先TnpB和后代Cas12的特征,在進(jìn)化樹上位于兩者之間,是名副其實(shí)的“過渡化石” 。
2.揭示“雙模”引導(dǎo)的功能過渡性
功能實(shí)驗(yàn)證實(shí),TranC系統(tǒng)展現(xiàn)出獨(dú)特的“承前啟后”能力——它既能被祖先TnpB使用的reRNA引導(dǎo),也能被典型CRISPR系統(tǒng)的 CRISPR RNA(由tracrRNA和crRNA組成)引導(dǎo),進(jìn)行DNA切割,這一特性完美印證了其作為過渡態(tài)的身份。
3.冷凍電鏡直視“RNA分裂”的瞬間
研究通過高分辨率冷凍電鏡,首次解析了關(guān)鍵TranC蛋白與sgRNA、DNA的復(fù)合物結(jié)構(gòu)。結(jié)構(gòu)清晰地顯示,其引導(dǎo)RNA已經(jīng)呈現(xiàn)出由tracrRNA和crRNA組成的分離式架構(gòu),但在結(jié)構(gòu)上又與祖先TnpB的單一reRNA高度相似,直觀展示了RNA正在“分裂”的中間狀態(tài)。
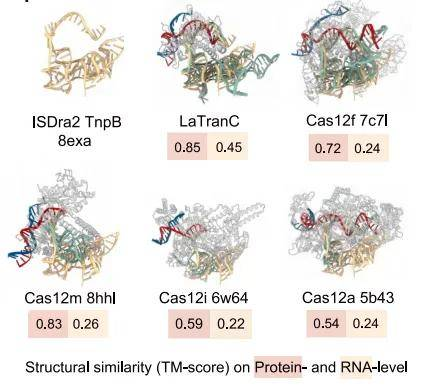
4.確立“RNA分裂”為關(guān)鍵進(jìn)化驅(qū)動(dòng)力
綜合進(jìn)化、結(jié)構(gòu)與功能證據(jù),本研究強(qiáng)有力地證明,功能性RNA分裂是驅(qū)動(dòng)從轉(zhuǎn)座子系統(tǒng)向CRISPR適應(yīng)性免疫系統(tǒng)轉(zhuǎn)變的關(guān)鍵一步。蛋白質(zhì)本身的改變并非主因,而是RNA指導(dǎo)機(jī)制的模塊化革新,催生了新的免疫功能
技術(shù)亮點(diǎn):捕獲“缺失的一環(huán)”
- 計(jì)算生物學(xué)挖掘:結(jié)合序列、結(jié)構(gòu)與模體三種方法,精準(zhǔn)識(shí)別TranC候選系統(tǒng)。
- 冷凍電鏡結(jié)構(gòu)解析:首次解析LaTranC-sgRNA-DNA復(fù)合物結(jié)構(gòu),揭示其與TnpB高度相似。
- 功能驗(yàn)證體系:在E. coli 和人類細(xì)胞中驗(yàn)證TranC系統(tǒng)的雙重引導(dǎo)RNA兼容性。
此項(xiàng)Cell 研究首次完整描繪了從轉(zhuǎn)座子到CRISPR系統(tǒng)的進(jìn)化路徑,將“RNA為中心”的進(jìn)化機(jī)制提升到新高度。所發(fā)現(xiàn)的TranC系統(tǒng)本身結(jié)構(gòu)緊湊、引導(dǎo)方式靈活,為開發(fā)新一代微型、可編程的基因編輯工具提供了寶貴的天然藍(lán)圖。
泓迅生物——精準(zhǔn)建庫與測序
在破解RNA結(jié)構(gòu)這一核心問題上,泓迅生物提供了重要的技術(shù)支持。泓迅生物的小RNA建庫技術(shù),無偏好性地捕獲樣本中小RNA片段,并通過高精度測序,清晰繪制出tracrRNA和crRNA的完整序列圖譜及其成熟末端,鎖定了RNA分裂發(fā)生的具體位置。

泓迅生物專利的Syno?合成技術(shù)平臺(tái),可以快速高效地實(shí)現(xiàn)sgRNA文庫構(gòu)建,并包裝成慢病毒混合文庫后轉(zhuǎn)染細(xì)胞。結(jié)合高通量/高內(nèi)涵篩選平臺(tái),利用控制細(xì)胞存活、結(jié)合免疫染色、流式細(xì)胞術(shù)等手段篩選得到所需細(xì)胞,最終通過測序等方法推斷出發(fā)揮作用的靶基因。其核心能力涵蓋從基因合成、sgRNA優(yōu)化設(shè)計(jì)、到細(xì)胞基因編輯驗(yàn)證的全流程解決方案。
- 針對(duì)客戶需求的模式物種進(jìn)行sgRNA設(shè)計(jì)
- 自由選擇sgRNA表達(dá)載體,提供轉(zhuǎn)染級(jí)質(zhì)粒
- 提供從sgRNA設(shè)計(jì)、文庫構(gòu)建到高通量篩選的一站式服務(wù)
本研究正是基礎(chǔ)科研與前沿生物技術(shù)公司協(xié)同創(chuàng)新的典范——泓迅以精準(zhǔn)的數(shù)據(jù)生成能力,助力科學(xué)家驗(yàn)證重大科學(xué)假說,共同推動(dòng)基因編輯工具的源頭創(chuàng)新與后續(xù)開發(fā)。
為什么選擇泓迅
領(lǐng)先的技術(shù)優(yōu)勢—AI密碼子優(yōu)化分析(專利技術(shù))
更高的價(jià)值服務(wù)—合成生物學(xué)一站式解決方案

[1] Jin S, Zhu Z, Li Y,et al. Functional RNA splitting drove the evolutionary emergence of type V CRISPR-Cas systems from transposons. Cell. 2025 Oct 30;188(22):6283-6300.e22.
 Syno?C 引物合成
Syno?C 引物合成 RNA合成
RNA合成 mRNA合成
mRNA合成 Syno?GS 基因合成
Syno?GS 基因合成 載體構(gòu)建
載體構(gòu)建 高通量及DNA文庫構(gòu)建
高通量及DNA文庫構(gòu)建 CRISPR基因編輯平臺(tái)
CRISPR基因編輯平臺(tái) 病毒包裝
病毒包裝 基因測序及分析
基因測序及分析 重組蛋白表達(dá)平臺(tái)
重組蛋白表達(dá)平臺(tái) 抗體工程平臺(tái)
抗體工程平臺(tái) 多肽服務(wù)
多肽服務(wù) 生物信息學(xué)分析與設(shè)計(jì)
生物信息學(xué)分析與設(shè)計(jì) CRISPR文庫
CRISPR文庫 合成生物學(xué)產(chǎn)品
合成生物學(xué)產(chǎn)品 ProXpress蛋白快速檢測
ProXpress蛋白快速檢測 CRISPR 質(zhì)粒
CRISPR 質(zhì)粒





















