重磅 | 新一代RNA療法重塑罕見病治療的未來
序言
家族性乳糜微粒血癥(FCS)是一種嚴(yán)重的罕見疾病。據(jù)估計(jì),美國有6500人(百萬分之一至百萬分之二)患有遺傳或臨床FCS,其特征是甘油三酯水平可能比正常水平高10至100倍,導(dǎo)致發(fā)生急性,復(fù)發(fā)性和潛在致命性胰腺炎的風(fēng)險(xiǎn)大大增加。
2025年11月18日 (加州帕薩迪納) Arrowhead Pharmaceuticals, Inc.宣布,美國食品藥品監(jiān)督管理局 (FDA) 已批準(zhǔn)小干擾 RNA (siRNA) 藥物 REDEMPLO(plozasiran)普樂司蘭鈉注射液作為飲食療法的輔助手段,用于降低家族性乳糜微粒血癥 (FCS) 成人患者的甘油三酯水平。REDEMPLO是FDA批準(zhǔn)的第一種也是唯一一種針對FCS患者的siRNA藥物,可以在家中自我管理,每三個(gè)月進(jìn)行一次簡單的皮下注射。REDEMPLO(plozasiran)是一種小干擾RNA(siRNA)治療劑,靶向APOC3基因,該基因編碼載脂蛋白C-III(apoC III)蛋白。載脂蛋白C III在肝臟中產(chǎn)生,并通過減緩甘油三酯的分解和清除來提高甘油三酯水平。通過沉默APOC3,Redemplo可顯著降低家族性乳糜微粒血癥綜合征(FCS)患者的甘油三酯并降低急性胰腺炎的風(fēng)險(xiǎn)。
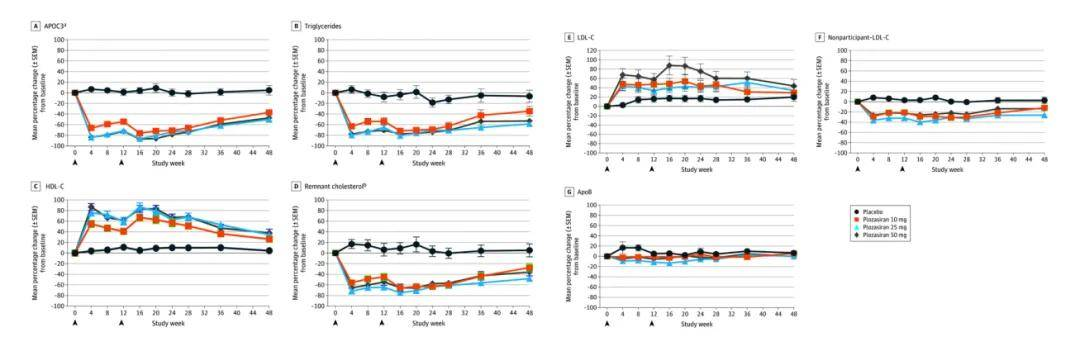
Plozasiran給藥48周脂質(zhì)和脂蛋白的變化[1]
FDA的一紙批準(zhǔn),再次讓類似(FCS)的極罕見疾病走進(jìn)大眾視野。全球行業(yè)的目光聚焦于新藥REDEMPLO(plozasiran),這不僅是一款新療法,更是RNA干擾(RNAi)療法從科學(xué)概念邁向普惠醫(yī)療的一個(gè)里程碑。患者僅需每三個(gè)月在家中自行皮下注射一次,即可顯著降低危及生命的超高甘油三酯水平,預(yù)防致命性胰腺炎。這背后,是一場持續(xù)近二十年的、關(guān)于如何讓RNA分子成為精準(zhǔn)醫(yī)療利器的技術(shù)革命。
RNA療法的轉(zhuǎn)變
從“不可成藥”到“精準(zhǔn)狙擊”
傳統(tǒng)小分子藥物和抗體藥通常靶向蛋白質(zhì),但許多疾病根源在于基因的異常表達(dá)。對于由特定基因過度表達(dá)引起的罕見病,直接沉默其信使RNA(mRNA)是更根本的策略。RNA療法,特別是小干擾RNA(siRNA),正是這樣的“基因剪刀手”,能在轉(zhuǎn)錄后水平精準(zhǔn)降解靶標(biāo)mRNA,從源頭阻止致病蛋白的產(chǎn)生。

人工合成小干擾RNA ( siRNA )介導(dǎo)的敲低機(jī)制示意圖[2]
第一代siRNA藥物(如2018年獲批的Patisiran)證明了該路徑的可行性,但其早期挑戰(zhàn)也很明顯:穩(wěn)定性差、易被降解、需要復(fù)雜的脂質(zhì)納米粒(LNP)包裹并通過靜脈頻繁給藥,且主要局限于肝臟靶向。
技術(shù)驅(qū)動的迭代
第二代siRNA的核心突破
REDEMPLO所代表的第二代siRNA療法,標(biāo)志著多項(xiàng)核心技術(shù)的成熟與整合,解決了初代產(chǎn)品的關(guān)鍵瓶頸:
化學(xué)修飾的飛躍:通過廣泛而精確地引入2′-O-甲基、2′-氟代等糖環(huán)修飾以及硫代磷酸酯骨架,大幅增強(qiáng)了RNA分子的核酸酶抗性,延長了其在體內(nèi)的半衰期,實(shí)現(xiàn)了從“月”到“季”甚至更長的給藥間隔。
設(shè)計(jì)規(guī)則的深化:對siRNA雙鏈結(jié)構(gòu)(如鏈長、末端化學(xué))、正義鏈與反義鏈的負(fù)載優(yōu)化,以及更精細(xì)的化學(xué)修飾模式,共同提升了其進(jìn)入RNA誘導(dǎo)沉默復(fù)合體(RISC)的效率,在增強(qiáng)療效的同時(shí),最大限度地降低了脫靶效應(yīng)和免疫原性風(fēng)險(xiǎn)。
靶向遞送的進(jìn)化:GalNAc(N-乙酰半乳糖胺)遞送系統(tǒng)的優(yōu)化是推動肝靶向siRNA成功商業(yè)化的關(guān)鍵。通過將siRNA與特異性結(jié)合肝細(xì)胞表面ASGPR受體的GalNAc配體共價(jià)連接,實(shí)現(xiàn)了高效、特異的肝臟攝取。第二代GalNAc技術(shù)親和力更高,使得皮下注射即可達(dá)到強(qiáng)效持久的基因沉默,極大提升了患者依從性和生活質(zhì)量。
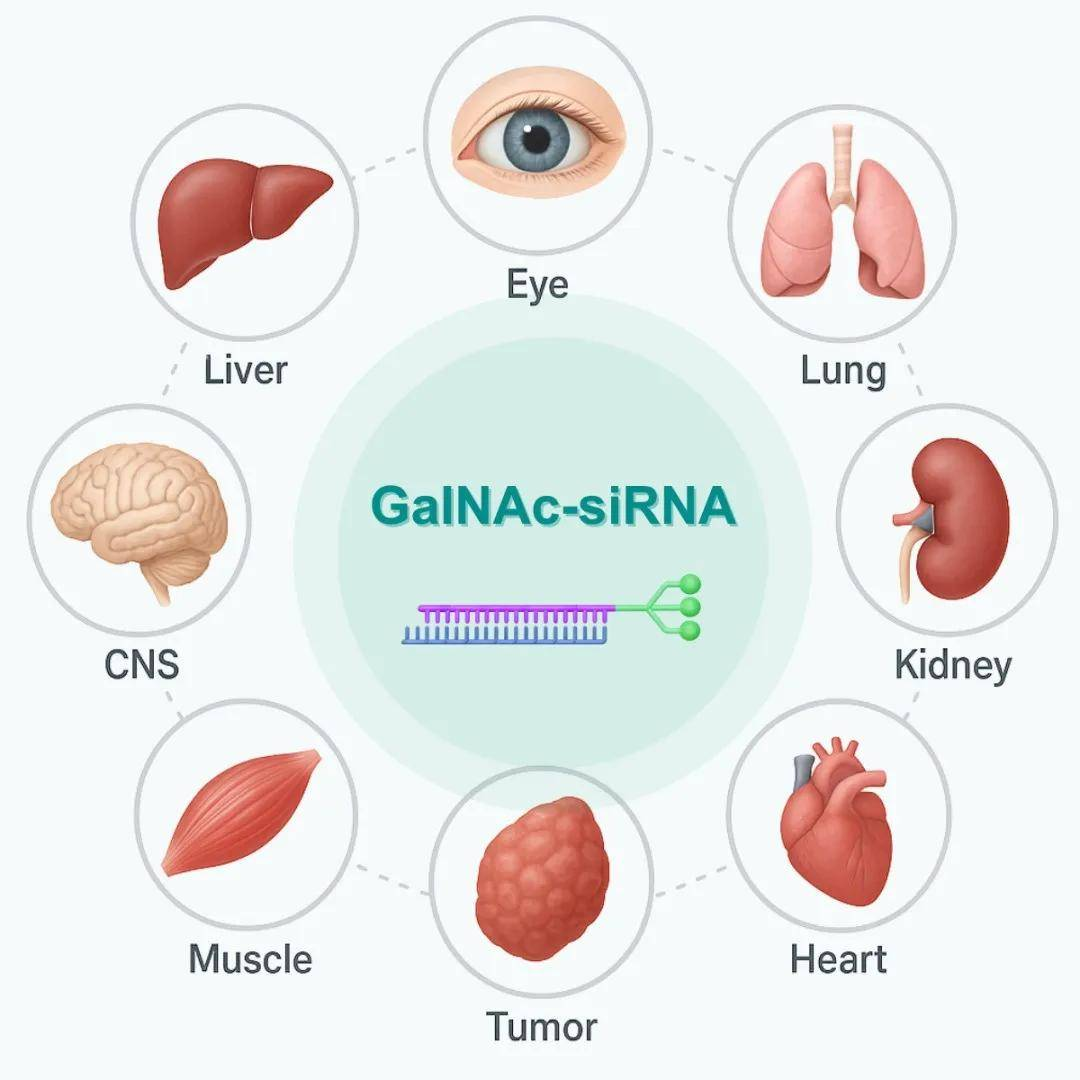
超越肝臟
罕見病治療的新邊疆
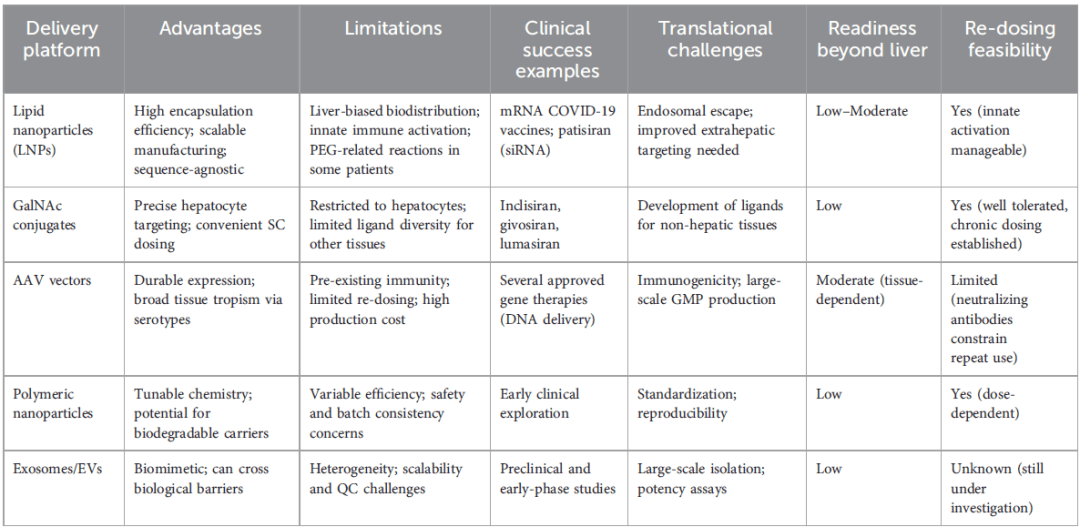
當(dāng)前獲批的RNA療法大多聚焦于肝臟表達(dá)的靶點(diǎn)。然而,罕見病的挑戰(zhàn)遠(yuǎn)不止于此。中樞神經(jīng)系統(tǒng)(CNS)、肌肉、眼部等組織的疾病,急需突破遞送壁壘。行業(yè)的前沿?zé)狳c(diǎn)正聚焦于:
血腦屏障(BBB)穿梭技術(shù):開發(fā)新型肽段、抗體或適配體作為“特洛伊木馬”,幫助RNA藥物進(jìn)入大腦,為亨廷頓病、肌萎縮側(cè)索硬化癥(ALS)等神經(jīng)退行性疾病帶來希望。
肌肉與心臟靶向:通過新型脂質(zhì)或配體偶聯(lián),將藥物精準(zhǔn)遞送至肌纖維或心肌細(xì)胞,拓展杜氏肌營養(yǎng)不良、遺傳性轉(zhuǎn)甲狀腺素蛋白淀粉樣變性(ATTR)心肌病等的治療選擇。
新型RNA模態(tài)的探索:除了siRNA,反義寡核苷酸(ASO) 在剪接修飾(如脊髓性肌萎縮癥治療)上已獲成功,而mRNA療法和環(huán)狀RNA等新興平臺,則為補(bǔ)充功能性蛋白或進(jìn)行更復(fù)雜的調(diào)控提供了全新工具箱。
泓迅生物
賦能下一代RNA解決方案
在這場由技術(shù)驅(qū)動的醫(yī)療變革中,從靶點(diǎn)發(fā)現(xiàn)到最終藥品的生產(chǎn),每一個(gè)環(huán)節(jié)都離不開精密的設(shè)計(jì)與可靠的制造。作為深耕合成生物學(xué)與核酸技術(shù)多年的專家,泓迅生物致力于為全球合作伙伴提供從序列設(shè)計(jì)優(yōu)化、高級化學(xué)修飾核苷酸合成、到工藝開發(fā)與規(guī)模化生產(chǎn)的一站式RNA解決方案。
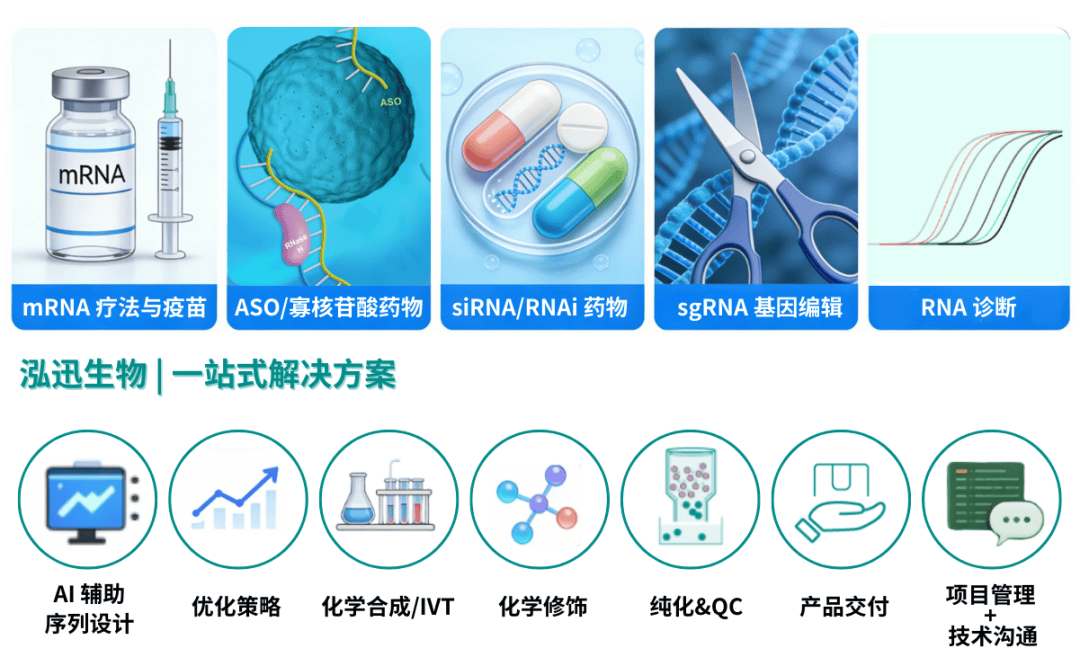
我們深刻理解,一個(gè)成功的RNA藥物分子,是其生物信息學(xué)設(shè)計(jì)、化學(xué)修飾策略、遞送系統(tǒng)適配及生產(chǎn)工藝的完美統(tǒng)一。
泓迅生物憑借在核酸化學(xué)、酶學(xué)工藝和質(zhì)控分析上的深厚積累,助力合作伙伴加速從靶點(diǎn)驗(yàn)證到臨床前研究乃至商業(yè)化生產(chǎn)的進(jìn)程,共同將更多如REDEMPLO般改變生命的療法,帶給亟待希望的罕見病患者群體。
結(jié)語
從每幾周一次的靜脈輸注,到每季度一次的家庭皮下注射;從治療單一肝病,到向中樞神經(jīng)、心血管等復(fù)雜系統(tǒng)進(jìn)軍——RNA療法的進(jìn)化史,是一部技術(shù)創(chuàng)新驅(qū)動醫(yī)療普惠的史詩。隨著遞送技術(shù)的持續(xù)突破和化學(xué)修飾的日益精進(jìn),我們有理由相信,未來十年,RNA療法將為更多“無藥可醫(yī)”的罕見病,點(diǎn)亮一盞明燈。
Reference
[1] Gaudet D, Pall D, et al. Plozasiran (ARO-APOC3) for Severe Hypertriglyceridemia: The SHASTA-2 Randomized Clinical Trial. JAMA Cardiol. 2024 Jul 1;9(7):620-630.
[2] Friedrich M, Aigner A. Therapeutic siRNA: State-of-the-Art and Future Perspectives. BioDrugs. 2022 Sep;36(5):549-571.
 Syno?C 引物合成
Syno?C 引物合成 RNA合成
RNA合成 mRNA合成
mRNA合成 Syno?GS 基因合成
Syno?GS 基因合成 載體構(gòu)建
載體構(gòu)建 高通量及DNA文庫構(gòu)建
高通量及DNA文庫構(gòu)建 CRISPR基因編輯平臺
CRISPR基因編輯平臺 病毒包裝
病毒包裝 基因測序及分析
基因測序及分析 重組蛋白表達(dá)平臺
重組蛋白表達(dá)平臺 抗體工程平臺
抗體工程平臺 多肽服務(wù)
多肽服務(wù) 生物信息學(xué)分析與設(shè)計(jì)
生物信息學(xué)分析與設(shè)計(jì) CRISPR文庫
CRISPR文庫 合成生物學(xué)產(chǎn)品
合成生物學(xué)產(chǎn)品 ProXpress蛋白快速檢測
ProXpress蛋白快速檢測 CRISPR 質(zhì)粒
CRISPR 質(zhì)粒





















